1.хімічний зв'язок, який утворений за спільних електронних пар називається:
а) ковалентний, б) йонний, в) металічний
2.якщо атоми, які взаємодіють між собою мають різну електронегативність, то утворюється
ковалентний зв'язок: а) полярний, б) неполярний.
3.вкажіть ря, в якому елементи розташовані в порядку зростання електронегативності:
а) i, br.ci б) c, si, ge b) n, p, as
4.вкажіть формулу сполуки з ковалентним неполярним зв'язком:
а) 0, б) naci b) hci г) nh; д) к
5. вкажіть формуту сполуки з йонним зв'язком:
а) 0,
б) naci,
b) hci
t) nhẹ 1
6. вкажіть формули спотук з ковалентним полярним зв'язком:
а) 0, б) naci в) hci г) nh; д) к
-
8 атом якого елемента має на два електорни менше, ніж йон кальцію?
пn inr 18 електронів та 19 протонів. назвіть
CH₃COOH + C₂H₅OH = CH₃COOC₂H₅ + H₂O
1) Найдем количества каждого из реагирующих веществ, чтоб узнать, какое вещество дано в избытке:
M(CH₃COOH)=60 г/моль
M(C₂H₅OH)=46 г/моль
(уже, кстати, из молярных масс очевидно, что спирт дан в избытке, но мы все равно это проверим)
n(CH₃COOH)=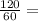 2 моль
2 моль
n(C₂H₅OH)=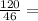 2,6 моль
2,6 моль
2) Расчет проводим по уксусной кислоте
M(CH₃COOH)=60 г/моль
M(CH₃COOC₂H₅)= 88 г/моль
m(CH₃COOH)= 120 г
m(CH₃COOC₂H₅)= х г
Расчет по уравнению реакции:
60 г CH₃COOH дают 88 г CH₃COOC₂H₅
120 г CH₃COOH дают х г CH₃COOC₂H₅
3) Найдем реальных выход эфира через пропорцию:
176 г - это 100% выхода
у г - это 80% выхода
ответ: можно получить 140,8 г эфира.
С водой взаимодействует только сульфид алюминия - с выделением сероводорода.
С кислотой реагирует и Al2S3 и Al.
В последнем случае выделяется и сероводород (в том же кол-ве, что и в реакции с водой), и водород.
Объём водорода - разность объёма смеси газов и объёма сероводорода:
V(H2S) = 6,72 (л)
V(H2) 13,44 - 6,72 = 6,72 (л)
Объёмы газов у нас есть.
Теперь надо определить количество, а затем - массу веществ.
n(H2) = n(H2S) = 6,72/22,4 = 0,3 (моль)
Al2S3 + 6H2O --> 2Al(OH)3 ↓ + 3H2S↑
n(Al2S3) = n(H2S) * 1/3 = 0,1 (моль)
m(Al2S3) = 0,1 * 150 = 15 (г)
2Al + 6HCl --> 2AlCl3 + 3H2
n(Al) = n(H2) * 2/3 = 0,2 (моль)
m(Al) = 27* 0,2 = 5,4 (г)
W(Al) = 5,4/20,4 = 0,2647
или в процентах:
26,47 ~ 26,5 %