Железо имеет покрытие из Ni и Ag . Какой из металлов (железо или покрытие) будет подвергаться коррозии в случае нарушения поверхностного слоя покрытия в условиях влажной промышленной атмосферы. Составьте схемы процессов, происходящих на электродах образующихся гальванических элементов.
Оксид этого металла имеет формулу X2O3, где X это металл.
Нитрат этого оксида имеет формулу X(NO3)3.
30,6г *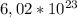 * 3 = 21,3г *
* 3 = 21,3г * 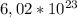 * 9
* 9
(2z+48)г/моль (z+186)г/моль
30,6 *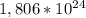 = 21,3 *
= 21,3 * 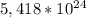
(2z+48) (z+186)
z ≈ 27
Такая атомная масса у алюминия. Проверим.
30,6г *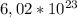 * 3 = 21,3г *
* 3 = 21,3г * 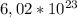 * 9
* 9
(54+48)г/моль (27+186)г/моль
0,3 *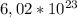 * 3 = 0,1 *
* 3 = 0,1 * 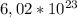 * 9
* 9
Идеально! Значит X = Al
Объяснение:
1. Яку кількість речовини становить алюміній оксид Al2O3масою 306 г.
n(Al2O3)= m/M= 306/(2•27+3•16)=306/102=3моль
2. Обчисліть масу фосфор (V) оксиду кількістю речовини 1,5 моль.
m(P2O5)= n×M= 1.5•(2•31+5•16)= 1.5•142= 213г
3. Яку кількість речовини становлять 3×1023атоми Оксигену?
n(O2)=N/Na = 3•10²³/6.02•10²³=0.5моль
4. Обчисліть відносну густину карбон (ІІ) оксиду за азотом.
D= M(CO)/M(N2)=(12+16)/(2•14)=28/28=1
5. Обчисліть масу кисню, об’ємом 2.8л.(н.у.)
m(O2)= n×M= (V/Vm)×M= (2.8/22.4)×(2•16)= 0,125•32 = 4г
6. Обчисліть молярну масу газу, якщо його відносна густина за воднем дорівнює 35,5.
M(газу)= D×M(H2)=35.5•2•1= 71г/моль