Выбери верное утверждение о «массовой доли» вещества в растворе:
А) отношение массы раствора к массе растворенного вещества
Б) отношение массы раствора к его объёму
В) отношение массы растворенного вещества к массе раствора
Г) отношение массы растворителя к массе раствора
2. Для вычисления массы растворенного вещества нужно использовать следующую формулу
А) W= m (растворенного вещества) * 100%
m (раствора)
Б) m(растворенного вещества) = w* m (раствора)
В) m = n*M
Г) m (раствора) = m(растворенного вещества)
w
3. Выберите правильное утверждение о чистых веществах:
А) это только вещества
Б) это вещества, состоящие из нескольких компонентов
В) это вещества, состоящие только из одного компонента
Г) это только сложные вещества
4. Из данных смесей выберите
А) жидкие, Б) твердые, В) газообразные
Воздух, уксус, природный газ, бронза, речная вода, ртуть, сталь, дистиллированная вода
5. Каким можно разделить смесь воды и растительного масла?
А) Фильтрованием Б) С магнита
В) Отстаиванием с последующим отделением в делительной воронке
II. Решение расчётных задач «Массовая доля растворенного вещества»
1. В 100г воды растворили 5г сахара. Найдите массовую долю сахара в данном растворе.
2. Определите массу поваренной соли, содержащегося в 300г 8%-ого раствора.
3. К 30 г 20% раствора поваренной соли добавили 15 мл воды. Вычислите массовую долю полученного раствора.
3. Во-первых, мы сразу видим что это химическая формула соли угольной кислоты и кальция. По другому, мы её ещё называем - карбонат кальция. Видим качественный(состоит из трех химических элементов: Ca, C, O) и количественный - в состав входит 1 атом кальция(Ca), 1 атом углерода(C) и 3 атома кислорода(O), составы. Молярную массу, равную 100 г/моль: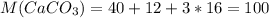 г/моль. Массовую долю всех химических элементов в составе соли:
г/моль. Массовую долю всех химических элементов в составе соли: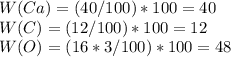
Соотношение массы хим.элементов: 40:12:48
4. Простые вещества - вещества, состоящие из одного хим.элемента.
Подходят: Б) озон , В) железо
, В) железо  ;
;
5. О простом веществе: Б, Г;
О хим.элементе: А, В, Д
1) AgNO3+NaCl=AgCl+NaNO3 - Видим нерастворимую соль - показатель РИО
Ag⁺+NO₃⁻ + Na⁺ + Cl⁻ = AgCl+ Na⁺+ NO₃⁻
Ag⁺+Cl⁻=AgCl↓
2) Ba(OH)2+2HNO3=Ba(NO3)2+2H2O - Образуется слабый электролит - вода, значит РИО
Ba²⁺+2OH⁻+2H⁺+2NO3⁻ = Ba²⁺+2NO3⁻+2H2O
OH⁻+H⁺=H2O
3) Na2CO3+2HCl=2NaCl+CO2+H2O - Образуются оксиды - неэлектролиты, РИО
2Na⁺+CO3²⁻ + 2H⁺+2Cl⁻= 2Na⁺ + 2Cl⁻ + CO2 + H2O
CO3²⁻+2H⁺=CO2+H2O
4) Na2SiO3+H2SO4=Na2SO4+H2SiO3 - Нерастворимая кислота H2SiO3, РИО
2Na⁺+SiO3²⁻+2H⁺+SO4²⁻=2Na⁺+SO4²⁻+H2SiO3
SiO3²⁻+2H⁺=H2SiO3
5) K2S+H2SO4=K2SO4+H2S - Слабые электролит, РИО
2K⁺+S²⁻+2H⁺+SO4²⁻=2K⁺+SO4²⁻+H2S
S²⁻+2H⁺=H2S
6) 2KCl+Na2SO4=2NaCl+K2SO4 - Все растворимо, не РИО
Таким образом, все, за исключением последней реакции - реакции ионного обмена
Объяснение: