ВАРИАНТ I 1
Составьте определение алканов, вставив вместо пропусков (1) - (5) термины или
формулы, перечисленные под буквами а – м в соответствующих падеже и числе.
Определение запишите в тетради.
Алканы – это (1) углеводороды с (2) цепью атомов углерода, в молекулах
которых имеются только (3) связи между атомами углерода. Состав их соответствует
общей формуле (4) . Для них характерны реакции (5) .
a)
CnH2n-2; ж) тройные;
б) циклическая; з) предельный;
в) двойные; и) простые;
г) CnH2n+2; к) CnH2n;
д) открытая; л) замещения;
е) непредельный; м) присоединения.
Гомологический ряд – это ряд веществ
а) отличающихся построению и свойствам
б) сходных построению и свойствам
в) отличающихся по составу на одну или несколько групп СН2
г) имеющих одинаковый состав
Общая формула алканов
а) CnH2n-6 в) СnH2n-2
б) CnH2n г) CnH2n+2
Формула алкенов
а) C5H12 в) С3Н4
б) С2Н4 г) С4Н10
Структурная формула алкана
а) СН2═СН─СН3 в) Н2С─СН2
│ │
Н2С─СН2
б) СН3─СН─СН─СН3 г) СН3─СН2─ОН
│ │
СН3 СН3
Формула алкила
а) СН3─СН─СН2─СН3 в) СН3─СН═СН─СН3
│
б) СН4 г) НО ─СН2─СН3
Название алкена
а) пентен в) пропин
б) пропан г) метан
Соотнесите
Н а з в а н и е Ф о р м у л а
1) гексан а) СН═СН─(СН2)3─СН3 д) СН3─СН─СН3
2) этил б) СН3─СН2─ │
3) пропан в) СН3─СН2─СН3
4) гексен г) СН3─(СН2)4─СН3 е) СН3─СН3
5) этан
6) пропил
решите ответов так и не нашёл
Объяснение:
При нагревании до 180° С в умеренном количестве кислорода образуется оксид натрия:4Na + O2 = 2Na2O
2. Натрий горит на воздухе с образованием пероксида натрия:
2Na + O2 = Na2O2
Натрий хранят под слоем керосина.
3. Расплавленный натрий в хлоре сгорает с ослепительной вспышкой (можно говорить проще — реагирует с хлором при нагревании), на стенках сосуда образуется белый налет хлорида натрия:
2Na + Cl2 = 2NaCl
4. Натрий может взрываться при растирании с порошком серы (образуется сульфид натрия):
2Na + S = Na2S
5. Натрий при нагревании восстанавливает водород, образуется гидрид натрия:
2Na + H2 = 2NaH
Объяснение:
1. З нерозчинним у воді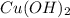 блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
Висновок: для якісного визначення глюкози використовують важкі метали.
2. Етаналь можна визначити за до реакції "срібного дзеркала":
СН3-СНО + 2[Ag(NH3)2OH = CH3COOH + 2Ag(осад) + 4NH3 + H2O
на стінках пробірки утворюється тонкий шар срібла.
Висновок: для виявлення альдегідів можна узяти аміачний розчин аргентум(І) оксиду
Сахарозу можна виявити за реакцією:
С12H22O11 + Ca(OH)2 = C12H22O11*CaO + H2O
Cпостереження: утворення безбарвного розчину кальцій сахариту
Висновок: для виявлення сахарози необхідно узяти кальцій гідроксид
3. Для виявлення гідроксильної групи:
прикладаю фото
утворюється прозорий розчин купрум(ІІ) глюконату синього кольору
Для виявлення альдегідної групи:
CH2OH-(CHOH)4--CHO + Cu(OH)2 =(нагрівання) CH2OH-(CHOH)4-COOH + CuOH + H2O
За подальшого нагрівання утворюється осад цегляно-червоного кольору:
2CuOH = Cu2O(ocaд) + Н2О
блакитний купрум (ІІ) гідроксид розчиниться, а замість нього утвориться оранжевий осад купрум (І) гідроксиду, який за подальшого нагрівання набуде цегляно-червоного кольору.
Висновок: Щоб виявити глюкозу нам необхіден такий реактив як купрум (ІІ) гідроксид. Зазначимо те, що для виявлення альдегідної групи треба здійснити нагрівання