.. вариант 1
1.общее число атомных орбиталей на третьем энергетическом уровне равно:
а) 9 б) 8 в)6 г)3
2. элементы перечислены в порядке уменьшения радиуса атома в ряду:
а) алюминий, натрий, кремний б) натрий, алюминий, кремний
в) кремний, алюминий, натрий г) натрий, кремний, алюминий
3. наиболее выраженные кислотные свойства имеет оксид:
а) cl2o7 б) so2 в) so3 г) al2o3
4. количество теплоты (в кдж), которое выделяется при растворении 100 г оксида меди(ii) в избытке хлороводородной кислоты в соответствии с уравнением
cuo(т) + 2hcl(ж)= cucl2(р-р) +h2o(ж) + 63,93 кдж, равно
а) 56 б) 62 в) 80 г) 94
5. связь между молекулами воды:
а) ионная б) водородная
в) ковалентная полярная д)ковалентная неполярная
6. реакция co(г) +cl2(г) ↔ cocl2(г) –q протекает в замкнутом объёме. равновесие этой системы смещается в сторону исходных веществ при:
а) увеличении концентрации оксида углерода (ii)
б) увеличении концентрации хлора
в) увеличении давления
г) уменьшении температуры
7.температурный коэффициент реакции γ =3. при увеличении температуры на 400 с скорость реакции возрастёт в:
а) 120 раз б) 12 раз в) 81 раз г) 27 раз
8. подвергается гидролизу соль:
а) сульфат натрия б)бромид калия
в) сульфид натрия г) хлорид калия
9. в водном растворе щелочная среда образуется при гидролизе соли:
а) нитрата калия б) карбоната калия
в) хлорида железа (iii) г) хлорида аммония
10.сокращённое ионное уравнение pb2+ + so42- =pbso4 соответствует реакции
а) сульфида свинца(ii) с серной кислотой
б) гидроксида свинца(ii) c cерной кислотой
в) оксида свинца(ii) с серной кислотой
г)нитрата свинца(ii) с сульфатом аммония
11. в результате диссоциации по первой ступени мышьяковой кислоты h3aso4, образуются ионы:
а)aso43- и h+ б) haso42- и h+ в)h2aso4- и h+ г) aso43- и oh-
12. в водном растворе возможна реакция между:
а) гидроксидом калия и нитратом натрия
б) гидрофосфатом калия и гидроксидом калия
в) хлоридом алюминия и соляной кислотой
г) нитратом железа (ii) и хлоридом калия
13. сумма стехиометрических коэффициентов в уравнении окислительно-восстановительной реакции
sncl2 + kmno4 + h2so4 → sn(so4)2 + mnso4 +sncl4 +…+…. равна
а) 19 б)69 в)32 г)44
Відповідь:
а) Na2SO4 + BaCl2 ⇒ 2NaCl + BaSO4↓;
б) Na2CO3 + 2HCl ⇒ NaCl + CO2↑ + H2O;
в) отсутствует.
Пояснення:
Для того чтобы решить это задание нужно написать формулы всех веществ и посмотреть с каких ионов они состоят:
сульфата натрия - Na2SO4 (Na+ и SO4 2-)
хлорида бария - BaCl2 (Ba2+ и 2Cl-) и т.д.
карбоната натрия - Na2CO3
сульфата меди (II) - CuSO4
сульфида натрия - Na2S
хлорида алюминия - AlCl3
хлорида натрия - NaCl
хлорида железа (III) - FeCl3
гидроксида натрия - NaOH
соляной кислоты - HCl.
Потом нужно открыть таблицу «Растворимость кислот, оснований и солей в воде» и посмотреть к чему приведет взаимодействие (по реакции обмена) каждого вещества с каждым. Но при этом сразу исключи взаимодействие веществ с одинаковыми ионами или анионами. У тебя же не будет взаимодействовать например Na2S + NaCl, или BaCl2 + NaCl. Все остальные реакции перемотри в таблице и выпиши на листок. Потом продукты проверь в таблице: если на пересечении аниона и иона будет "р" - вещество растворимое, если "м" - малодиссоциирующее, если "н" - нерастворимое, если прочерк - соединение не существует, реакция не идет.
Я напишу по одному примеру к а), б) и в). Остальное попробуй найти сам/сама чтобы усвоить что надо делать.
а) осадок (нерастворимое вещество):
например Na2SO4 + BaCl2 ⇒ 2NaCl + BaSO4↓ (выпал в осадок, буква "н" в таблице). Также в таблице есть цвета - в ячейке этого вещества - цвет желтый и это означает что среда нейтральная (цвет ячейки может менятся в зависимости от таблицы в учебнике/интеренете). Но как мы можем определить среду экспериментально? Есть индикаторы: фенолфталеин, метилоранж, лакмус. Открываем таблицу индикаторов. Видим что в нейтральной среде, например при добавлении лакмуса - цвет расствора стает фиолетовый. Или при добавлении метил оранжа - оранжевый. Так и доказываем что среда нейтральная.
б) газ:
Тут немного посложнее, надо знать дополнительно в каких случаях образовывается газ. Самый класический - это если в результате взаимодействия двух веществ получается угольная кислота, которая не стойкая и всегда разлагается на углекислый газ (CO2) и воду (H2O).
Ищем в результате взаимодействия какиих веществ может образоваться угольная кислота (H2CO3), это:
Na2CO3 + 2HCl ⇒ 2NaCl + H2CO3 ⇒ NaCl + CO2↑ + H2O. Пока СО2 еще не полностью выделился среда расствора будет кислой, в экспериментальных условиях кислая среда проверяеся метилоржанжевым индикатором, который изменяет окрас с оранжевого на розовый.
в) малодиссоциирующее вещество (за тем же принципом что и вариант а, даже немного легче, т.к. буквы "м" в ячейках можно пересчитать на пальцах).
Если ты в условии все правильно написал/(а) по названиям то у тебя нет в веществах ионов и анионов прореагировать с образованием малодиссоциирующего вещества.
Но если ты невнимательно написал/(а) условие и там где-то сульфит, а не сульфат, то ответ будет.
Объяснение:
ТеорияЧисло молекул в количестве вещества связывает число Авогадро - число молекул вещества в его одном моле
Число Авогадро обозначается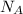 и оно равно
и оно равно 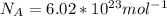
Количество вещества (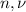 , допустимы обе записи) это отношение числа молекул (
, допустимы обе записи) это отношение числа молекул (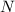 ) к числу молекул одного моля, числу Авогадро (
) к числу молекул одного моля, числу Авогадро (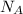 ):
):
Следовательно, чтобы найти число молекул нужно количество вещества умножить на число Авогадро:
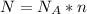
РешениеВыполним для нашей задачи, нам известно количество вещества уксусной кислоты, оно равно 0,1 моль (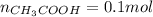 ) найдем число молекул
) найдем число молекул 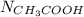 :
:
В десятой моль кислоты содержится столько молекул
ФормулыДругие формулы связывающие количество вещества и другие параметры: