1)1) Будет растворяться железо, т. к. его потенциал окисления-восстановления меньше(-0.44 В), чем у никеля(-0.25 В). Поэтому растворяться будет железо, а водородная деполяризация(т. е. выделение водорода, разрядка протонов) - на никеле.
2)Количество поглощенного водорода зависит от состояния поверхности металла и от температуры. Порошкообразные металлы и при температуре более высокой до известного предела поглощают больше водорода, чем сплошные и на холоду. Серебро, медь, железо, золото, платина в сплошном виде и при обыкновенной температуре поглощают на один объем металла менее одного объема водорода.
В одну стадию нельзя получить этиленгликоль из этанола, поэтому в каждом несколько реакций.
1. Получение по цепочке этанол ⇒ хлорэтан ⇒ винилхлорид ⇒ 1,2-дихлорэтан ⇒ этиленгликоль.
1. Реакция взаимодействия этанола с хлороводородом:
ᅠᅠ
2. Реакция дегидрирования хлорэтана при нагревании и в присутствии Никеля:
ᅠᅠ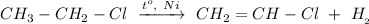
3. Реакция присоединения хлороводорода против правила Марковникова в присутствии пероксида водорода:
ᅠᅠ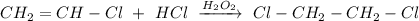
4. Щелочной гидролиз 1,2-дихлорэтана при нагревании водным раствором щёлочи, получаем этиленгликоль:
ᅠᅠ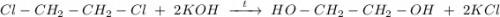
2. Получение по цепочке этанол ⇒ этен ⇒ эпоксид этилена ⇒ этиленгликоль.
1. Реакция внутримолекулярной дегидратации этанола при нагревании свыше 140 градусов и в присутствии концентрированной серной кислоты:
ᅠᅠ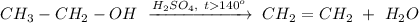
2. Реакция окисления этилена кислородом воздуха в присутствии ионов серебра:
ᅠᅠ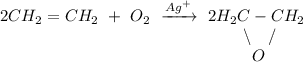
3. Гидролиз эпоксида в кислой среде при нагревании, получение этиленгликоля:
ᅠᅠ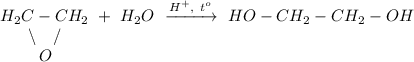
3. Получение по цепочке этанол ⇒ этилен ⇒ этиленгликоль.
1. Реакция внутримолекулярной дегидратации этанола при нагревании свыше 140 градусов и в присутствии концентрированной серной кислоты:
ᅠᅠ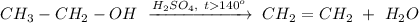
2. Реакция окисления этилена перманганатом калия в нейтральной среде при температуре в 0 градусов:
Объяснение:
1)1) Будет растворяться железо, т. к. его потенциал окисления-восстановления меньше(-0.44 В), чем у никеля(-0.25 В). Поэтому растворяться будет железо, а водородная деполяризация(т. е. выделение водорода, разрядка протонов) - на никеле.
2)Количество поглощенного водорода зависит от состояния поверхности металла и от температуры. Порошкообразные металлы и при температуре более высокой до известного предела поглощают больше водорода, чем сплошные и на холоду. Серебро, медь, железо, золото, платина в сплошном виде и при обыкновенной температуре поглощают на один объем металла менее одного объема водорода.
3)Электролиз расплава NaCl:
NaCl ⇄ Na+ + Cl-
K(-): Na+ + 1e → Na0
A(+): 2Cl- - 2e → Cl20
Вывод: 2NaCl → 2Na + Cl2