Короче, тут надо знать какой концентрации кислота, ибо реакции при разной концентрации протекают по-разному!
Ладно! Будем думать, что в первом случае у нас фосфорная кислота- безводная, т.е концентрация 100%, тогда составим уравнения реакции:
1) (При не очень высокой температуре)
2)Пишем в ионной форме: Сразу скажу, поскольку все соли растворимые, и кислоты, то в сокращённой ионной форме получится:
3)Для реакции с магнием, возьмём разбавленную фосфорную кислоту. Если надо реакции с концентрированной, то вот тебе правило: Чем выше концентрация фосфорной кислоты, тем больше атомов металла будут замещаться атомами водорода, т.е будут получаться кислые соли, например:
в данном случаем, магний заместил атомы водорода. В ходе данной реакции выпал осадок и выделился газ, запишем это в полной и сокращённой ионных формах:
Так! Электролиты- это соединения, которые проводят электрический ток!
Сильные- те которые, почти необратимо диссоциируют в растворе, а слабые- незначительно диссоциируют в растворе. Т.е все электролиты, должны быть растворимы в воде, а иначе никак!
1) Ba(OH)2 - сильный электролит, а NH4OH - слабый.
Электролитическая диссоциация этих оснований:
Ba(OH)2 = Ba2+ + 2OH-;
NH4OH = NH4+ + OH-;
2) Mg(OO)2 - вообще не является электролитом, поскольку нерастворим, а Ca(OH)2 - слабым электролитом, так малорастворим, он диссоциирует на ионы незначительно:
Ca(OH)2 = Ca2+ + 2OH-
3) Тут всё ясно, и KOH и Ba(OH)2- сильные электролиты, они полностью диссоциируют в растворе:
KOH = K+ + OH-;
Ba(OH)2 = Ba2+ + 2OH-;
Значит, эти два основания являются сильными электролитами.
4) Как уже говорил, Mg(OH)2- неэлектролит, а вот NaOH- сильный, потому что растворим. Вот, как раз он и необратимо продиссоциирует на ионы:
NaOH = Na+ + OH-
ответ: 3.
Редактор формул не работает, поэтому коряво! Думаю, разберёшься, что к чему!
Короче, тут надо знать какой концентрации кислота, ибо реакции при разной концентрации протекают по-разному!
Ладно! Будем думать, что в первом случае у нас фосфорная кислота- безводная, т.е концентрация 100%, тогда составим уравнения реакции:
1)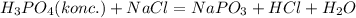 (При не очень высокой температуре)
(При не очень высокой температуре)
2)Пишем в ионной форме: Сразу скажу, поскольку все соли растворимые, и кислоты, то в сокращённой ионной форме получится:
3)Для реакции с магнием, возьмём разбавленную фосфорную кислоту. Если надо реакции с концентрированной, то вот тебе правило: Чем выше концентрация фосфорной кислоты, тем больше атомов металла будут замещаться атомами водорода, т.е будут получаться кислые соли, например: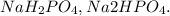
в данном случаем, магний заместил атомы водорода. В ходе данной реакции выпал осадок и выделился газ, запишем это в полной и сокращённой ионных формах:
Т.е магний восстановил водород.
Так! Электролиты- это соединения, которые проводят электрический ток!
Сильные- те которые, почти необратимо диссоциируют в растворе, а слабые- незначительно диссоциируют в растворе. Т.е все электролиты, должны быть растворимы в воде, а иначе никак!
1) Ba(OH)2 - сильный электролит, а NH4OH - слабый.
Электролитическая диссоциация этих оснований:
Ba(OH)2 = Ba2+ + 2OH-;
NH4OH = NH4+ + OH-;
2) Mg(OO)2 - вообще не является электролитом, поскольку нерастворим, а Ca(OH)2 - слабым электролитом, так малорастворим, он диссоциирует на ионы незначительно:
Ca(OH)2 = Ca2+ + 2OH-
3) Тут всё ясно, и KOH и Ba(OH)2- сильные электролиты, они полностью диссоциируют в растворе:
KOH = K+ + OH-;
Ba(OH)2 = Ba2+ + 2OH-;
Значит, эти два основания являются сильными электролитами.
4) Как уже говорил, Mg(OH)2- неэлектролит, а вот NaOH- сильный, потому что растворим. Вот, как раз он и необратимо продиссоциирует на ионы:
NaOH = Na+ + OH-
ответ: 3.
Редактор формул не работает, поэтому коряво! Думаю, разберёшься, что к чему!