19,4 г у л
100 г 22,4 л
1. Найдем чистую массу карбоната кальция в образца зная,что примесей 3%,а чистого карбоната будет 97%,то получим:
20 г - это 100%,а
х г_______97%, откуда г
2. Подставив в уравнение эту массу,получим:
при взаимодействии 100 г карбоната выделится 22,4 л, а
при -- // -- 19,4 г__________________у г, откуда
л (это ответ)
1)NaFCaCl2+2NaF===>2NaCl+CaF2(стрелка вниз,белый осадок)Ca(2+) + 2Cl(-) + 2Na(+) + 2F(-)> 2Na(+) + 2Cl(-) + CaF(стрелка вниз)Ca(2+) + 2F(-)===>CaF2) NaCl 2NaCl+Ag2SO4===>Na2SO4+2AgCl(стрелка вниз,выпадения белого,творожистого осадка)2Na(+) + 2Cl(-) + 2Ag(+) + SO4(2-)===>2Na(+) + SO4(2-) + 2AgCl(стрелка вниз)2CL(-) + 2Ag(+) ===>2AgCl3)Na2SO4 Na2SO4+Ba(NO3)2===>BaSO4(стрелка вниз,выпадение белого нерастворимого в кислотах остатка)+2NaNO32Na(+) + SO4(2-) + Ba(2+) + 2NO3(-)===> BaSO4(стрелка вниз) + 2Na(+) + 2NO3(-)Ba(2+) + SO4(2-)===>BaSO4(стрелка вниз)
19,4 г у л
100 г 22,4 л
1. Найдем чистую массу карбоната кальция в образца зная,что примесей 3%,а чистого карбоната будет 97%,то получим:
20 г - это 100%,а
х г_______97%, откуда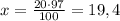 г
г
2. Подставив в уравнение эту массу,получим:
при взаимодействии 100 г карбоната выделится 22,4 л, а
при -- // -- 19,4 г__________________у г, откуда
1)NaF
CaCl2+2NaF===>2NaCl+CaF2(стрелка вниз,белый осадок)
Ca(2+) + 2Cl(-) + 2Na(+) + 2F(-)> 2Na(+) + 2Cl(-) + CaF(стрелка вниз)
Ca(2+) + 2F(-)===>CaF
2) NaCl
2NaCl+Ag2SO4===>Na2SO4+2AgCl(стрелка вниз,выпадения белого,творожистого осадка)
2Na(+) + 2Cl(-) + 2Ag(+) + SO4(2-)===>2Na(+) + SO4(2-) + 2AgCl(стрелка вниз)
2CL(-) + 2Ag(+) ===>2AgCl
3)Na2SO4
Na2SO4+Ba(NO3)2===>BaSO4(стрелка вниз,выпадение белого нерастворимого в кислотах остатка)+2NaNO3
2Na(+) + SO4(2-) + Ba(2+) + 2NO3(-)===> BaSO4(стрелка вниз) + 2Na(+) + 2NO3(-)
Ba(2+) + SO4(2-)===>BaSO4(стрелка вниз)