РЕБЯТ Найдите значение относительных атомных масс: алюминия, натрия, кислорода, железа, хлора
2. Найдите значение относительных манекулярных масс: Br2, H2O, CO2, H2SO4, KOH, BaS.
3. Рассчитайте массовые доли всех элементов в N205?
4. Охарактеризуйте фосфор, кальций, алюминий по плану:
1. символ
2. номер периода
3. номер группы
4. заряд ядра
5. колличество электронов.
2 H3C-CH(-OH)-CH3 + [ O ] ---> 2 H3C-CO-CH3 + H2O
пропанол-2: мол. масса = 60.1 г/моль; плотность = 0.785 г/см3 (проверьте пропанол указан в мл? )
ацетон: мол. масса = 58.08 г/моль
450 мл пропанола-2 = 450 * 0.785 = 353.25 грамм = (353.25 / 60.1) = 5.877 моль
2 моля пропанола-2 ---> 2 моля ацетона (по уравнению реакции)
5.877 моль пропанола-2 ---> 5.877 моля ацетона = 5.877 * 58.08 = 341.377 грамм (теоретический выход)
(300 / 341.377) * 100% = 88 % (87,88%) - практический выход
2 H3C-OH + [ O ] ---> 2 H-CO-H + H2O
200 мл метанола = 160 грамм = 160 / 32.04 = 5 моль
5 моль метанола ---> 5 моль формальдегида = 5 * 30.03 = 150 грамм
150 грамм чистого формальдегида приходится на 40% массы раствора
всего раствора (150 / 40) * 100 = 375 грамм или 375 / 1.1 = 340.9 мл
Объяснение:
1. З нерозчинним у воді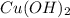 блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
Висновок: для якісного визначення глюкози використовують важкі метали.
2. Етаналь можна визначити за до реакції "срібного дзеркала":
СН3-СНО + 2[Ag(NH3)2OH = CH3COOH + 2Ag(осад) + 4NH3 + H2O
на стінках пробірки утворюється тонкий шар срібла.
Висновок: для виявлення альдегідів можна узяти аміачний розчин аргентум(І) оксиду
Сахарозу можна виявити за реакцією:
С12H22O11 + Ca(OH)2 = C12H22O11*CaO + H2O
Cпостереження: утворення безбарвного розчину кальцій сахариту
Висновок: для виявлення сахарози необхідно узяти кальцій гідроксид
3. Для виявлення гідроксильної групи:
прикладаю фото
утворюється прозорий розчин купрум(ІІ) глюконату синього кольору
Для виявлення альдегідної групи:
CH2OH-(CHOH)4--CHO + Cu(OH)2 =(нагрівання) CH2OH-(CHOH)4-COOH + CuOH + H2O
За подальшого нагрівання утворюється осад цегляно-червоного кольору:
2CuOH = Cu2O(ocaд) + Н2О
блакитний купрум (ІІ) гідроксид розчиниться, а замість нього утвориться оранжевий осад купрум (І) гідроксиду, який за подальшого нагрівання набуде цегляно-червоного кольору.
Висновок: Щоб виявити глюкозу нам необхіден такий реактив як купрум (ІІ) гідроксид. Зазначимо те, що для виявлення альдегідної групи треба здійснити нагрівання