1. К - элемент I группы главной подгруппы, у него ВСЕГДА на внешнем уровне 1 электрон, соответственно и степень окисления +1 (ему легче этот электрон отдать, чем 7 электронов принять). К ВСЕГДА обладает свойствами щелочных металлов (это типичный металл), значит он может образовывать ТОЛЬКО основные оксиды, формула высшего оксида К2О (общая формула высших оксидов находится в самом низу таблицы Менделеева под каждой группой, там вместо R в формуле подставляете элемент нужный, а все индексы сохраняете) Соответственно, свойства основных оксидов: а) реакция с водой К2О + Н2О = 2КОН б) с кислотами К2О + Н2SO4 = K2SO4 + H2O в) с амфотерными основаниями 3К2О+ 2Al(OH)3 = 2K3AlO3 + 3H2O г) с кислотными оксидами К2O + CO2 = K2CO3 2. гидроксид калия - щелочь (тривиальное название - едкое кали) - КОН
1. Речь идет о простом веществе водород: б) чистый водород спокойно горит;
2. Самый легкий газ:б) Н2;
3. В лаборатории водород получают при взаимодействии кислоты с:в) Zn;
4. Водород собирают вытеснения:г) воды, держа сосуд вверх дном.
5. «Гремучий газ» – смесь водорода с кислородом в соотношении: а) 2:1;
6. Массовая доля водорода в воде равна:г) 0,1
7. Реагирует с водородом при обычных температурах: б) Cl2;
8. Уравнение реакции и название продукта верны для:в) Н2 + О2 = Н2О, вода;
9. Относится к реакции восстановления: а) СuО + Н2 = Сu + Н2О;
10. Реактивами в цепочке превращений Сu СuО Сu являются: б) О2 и Н2;
11. Выберите формулу гидрида натрия:в) NaH;
12. Имеет самую низкую температуру кипения: б) Н2;
13. По термохимическому уравнению 2Н2 + О2 = 2Н2О + 571 кДж рассчитайте (в кДж) количество теплоты, выделившееся при сгорании 10 г Н2: в) 1427,5;
14. Сколько граммов кальция прореагирует с 4 г водорода: в) 80;
15.
16.Если колбы невозможно открыть,то определить можно по весу(на точных аналитических весах):какая из колб легче,там и водород.В ином случае,необходимо поднести тлеющую лучину,в которой вспыхнет-это кислород,в иной услышим хлопок-водород
1. К - элемент I группы главной подгруппы, у него ВСЕГДА на внешнем уровне 1 электрон, соответственно и степень окисления +1 (ему легче этот электрон отдать, чем 7 электронов принять). К ВСЕГДА обладает свойствами щелочных металлов (это типичный металл), значит он может образовывать ТОЛЬКО основные оксиды, формула высшего оксида К2О (общая формула высших оксидов находится в самом низу таблицы Менделеева под каждой группой, там вместо R в формуле подставляете элемент нужный, а все индексы сохраняете)
Соответственно, свойства основных оксидов:
а) реакция с водой
К2О + Н2О = 2КОН
б) с кислотами
К2О + Н2SO4 = K2SO4 + H2O
в) с амфотерными основаниями
3К2О+ 2Al(OH)3 = 2K3AlO3 + 3H2O
г) с кислотными оксидами
К2O + CO2 = K2CO3
2. гидроксид калия - щелочь (тривиальное название - едкое кали) - КОН
1. Речь идет о простом веществе водород: б) чистый водород спокойно горит;
2. Самый легкий газ:б) Н2;
3. В лаборатории водород получают при взаимодействии кислоты с:в) Zn;
4. Водород собирают вытеснения:г) воды, держа сосуд вверх дном.
5. «Гремучий газ» – смесь водорода с кислородом в соотношении: а) 2:1;
6. Массовая доля водорода в воде равна:г) 0,1
7. Реагирует с водородом при обычных температурах: б) Cl2;
8. Уравнение реакции и название продукта верны для:в) Н2 + О2 = Н2О, вода;
9. Относится к реакции восстановления: а) СuО + Н2 = Сu + Н2О;
10. Реактивами в цепочке превращений Сu СuО Сu являются: б) О2 и Н2;
11. Выберите формулу гидрида натрия:в) NaH;
12. Имеет самую низкую температуру кипения: б) Н2;
13. По термохимическому уравнению 2Н2 + О2 = 2Н2О + 571 кДж рассчитайте (в кДж) количество теплоты, выделившееся при сгорании 10 г Н2: в) 1427,5;
14. Сколько граммов кальция прореагирует с 4 г водорода: в) 80;
15.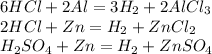
16.Если колбы невозможно открыть,то определить можно по весу(на точных аналитических весах):какая из колб легче,там и водород.В ином случае,необходимо поднести тлеющую лучину,в которой вспыхнет-это кислород,в иной услышим хлопок-водород