Почему индикаторы изменяют цвет в растворах кислот и оснований? напишите формулы и укажите заряды следующих ионов а) сульфат; б) ортофосфат; в) карбонат; г) бромид д) нитрат; е) силикат
напишите уравнение диссоциации следующих веществ а)HBr; б)NaNO3; в)BA(OH)2; г)ZnSO4; д)K3RO4; е)FeCI3.
3HMnO₄ + Al(OH)₃ = Al(MnO₄)₃ + 3H₂O тип: обмена
марганцовая кислота - гидроксид алюминия - перманганат алюминия - вода
CuO + H₂ = Cu + H₂O тип: замещение
оксид меди (II) - водород - медь - вода
CO₂ + CaO = CaCO₃ тип: соединение
оксид углерода (IV) - оксид кальция - карбонат кальция
Na₂SO₄ + BaCl₂ = BaSO₄ + 2NaCl тип: обмена
сульфат натрия - хлорид бария - сульфат бария -хлорид натрия
Al₂O₃ + 3H₂SO₄ = Al₂(SO₄)₃ + 3H₂O тип: обмена
оксид алюминия - серная кислота- сульфат алюминия -вода
2Al(OH)₃ = Al₂O₃ + 3H₂O тип: разложение
гидроксид алюминия - оксид алюминия - вода
Zn + 2HBr = ZnBr₂ + H₂ тип: замещение
цинк - бромоводороная кислота -бромид цинка - водород
2Rb + 2H₂O = 2RbOH + H₂ тип: замещение
рубидий - вода - гидроксид рубидия - водород
2H₃AsO₄ = As₂O₅ + 3H₂O тип: разложение
мышьяковистая кислота = оксид мышьяка (V) - вода
Объяснение:
кислоты: H₃AsO₄, H₂SO₄, HBr, H₃AsO₄
оксиды: CuO, H₂O,CaO, CO₂, Al₂O₃, As₂O₅
соли: Na₂SO₄, BaSO₄, NaCl, BaCl₂, Al₂(SO₄)₃, CaCO₃, Al(MnO₄)₃, ZnBr₂
основания: RbOH, Al(OH)₃,
х л 10 л
1.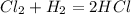
1 объем 1 объем
Согласно закона объемных отношений газов в реакции:
на 1 объем хлора необходимо 1 объем водорода,значит если взято 10 л водорода,то такой же объем и хлора необходимо взять для данной реакции,т.е.10 л
х г у 20 г
2.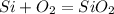
28 г 22,4 л 60 г
1. Находим массу кремния:
при взаимодействии 28 г кремния образуется 60 г его оксида,а
при -- // -- х г___________________20 г, откуда
х=28*20/60=9,3 г
2. Определяем объем кислорода:
при взаимодействии 22,4 л кислорода образуется 60 г оксида,а
при -- // -- у л_______________________20 г, откуда
у=22,4*20/60=7,5 л