Опыт два влияние площади соприкосновения реагирующих веществ. В одну пробирку насыпьте немного порошка мрамора, в другую - положите кристаллик и в обе пробирки прилить по 2 мл разбавленной соляной кислоты (1:2). В какой из пробирок реакция идёт быстрее и почему? Опыт третье влияние катализатора. В две пробирки налейте по 2 мл пероксида водорода H2O2, в одну из пробирок добавьте несколько Кристалликов оксида марганца(IV) MnO2. В какое из пробирок реакций идёт быстрее и почему?
и нужно сделать таблицу. Внесите тлеющую лучинку. Оформите работу в виде таблицы. В первом столбике: Рассматриваемый фактор, влияющий на скорость химической реакции, во втором: Описание эксперимента, в третьем: Наблюдения, позволяющие судить о скорости реакции, в четвёртом: уравнения реакции, в пятом: Вывод. Но ещё нужно сделать вывод по всей работе.
Вот, что я думаю по этому поводу...
1) Возьмём 1 атом кальция. Мы знаем его относительную атомную массу, а значит сможем найти и его абсолютную массу, т.к. ОАМ - это 1/12 часть АМ массы атома углерода или 100% от АМ водорода. Иными словами, Mr=Ar ; m(a) = Ar*m(a) H = Ar * 1/12 m(a) C
m(a) 40 * 1,67 *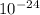 = 66,8 *
= 66,8 * 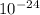 (г)
(г)
2) Зная реальную массу и плотность атома, сможем найти объём.
V = m : ρ = 66,8 *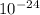 : 1,55 = 43,1 *
: 1,55 = 43,1 * 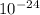 (
(
3) V факт. = 43,1 *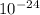 ( см^3 ) * 0,74 = 31,9 *
( см^3 ) * 0,74 = 31,9 * 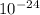 (см^3)
(см^3)
4) исходя из геометрических знаний, Vш = 4/3 * π *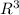 =>
=>
R =![\sqrt[3]{\frac{3V}{4* pi}}](/tpl/images/0140/1781/564c0.png) ~ 19,7 * 10^{-3}} см
~ 19,7 * 10^{-3}} см
ответ: R = 19,7 *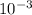 см, V = 31,9 *
см, V = 31,9 * 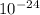 см^(3)
см^(3)
Бескислородные кислоты получают:
1. Взаимодействием неметалла с водородом.
Например:
H2 + Cl2 > 2HCl
2. Действием на соль более сильной или менее летучей кислотой.
Например:
FeS + 2HCl > FeCl2 + H2S
NaCl + H2SO4 ---> NaHSO4 + HCl
Кислородсодержащие кислоты получают:
1. Взаимодействием кислотных оксидов с водой.
Например:
SO3 + H2O > H2SO4
2. Действием на соль более сильной кислотой.
Например:
Na2SiO3 + H2SO4 > H2SiO3 + Na2SO4