а) У кислорода: если он стоит один то 0 (это у всех, не только у кислорода)
также есть -2 (чаще всего в соединениях он проявляет такую степень окисления) ,
-1 в ,
+2 в ,
так же может быть +4 в аллотропических модификациях кислорода.
б) У серы: -2 в сульфидах, гидросульфидах и сульфидокислотах,
если он стоит один то 0
+4 в тетрагалогенидах например,
+6 в соединениях с наиболее электроотрицательными элементами.
в) У азота: -3 в нитридах
-2 азот проявляет в соединениях перикисного типа,
в соединении под названием гидроксиламин он проявляет степень окисления -1
также может проявлять степени окисления +1 , ,
+3 и +5 в фториде, оксидах, оксогалогенидах.
г) Селенах: -2 в .
+4 селен проявляет в диоксиде, тетра- и оксогалогенидах
и в +6 это .
1) 2Al + 6HCl = 2AlCl3 + 3H2
2Al + 6H + 6Cl = 2Al + 6Cl + 6H
2) AlCl3 + 3NaOH = 3NaCl + Al(OH)3
Al + Cl3 + 3Na + 3OH = 3Na + 3Cl + Al(OH)3
Al + 3OH = Al(OH)3
3) 2Al(OH)3 = Al2O3 + 3H2O
2Al(OH)3 = 2Al + 3O + 3H2O
4) Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
2Al + 3O + 2Na + 2OH + 3H2O = 2Na + 2Al(OH)4
2Al + 3O + 2OH + 3H2O = 2Al(OH)4
5) 2Na[Al(OH)4] + 3Na2SO4 = Al2(SO4)3 + 8NaOH
2Na + 2Al(OH)4 + 6Na + 3SO4 = 2Al + 3SO4 + 8Na + 8OH
2Al(OH)4 = 2Al + 8OH
6) Al2(SO4)3 + 6NaOH = 2Al(OH)3 + 3Na2SO4
2Al + 3SO4 + 6Na + 6OH = 2Al(OH)3 + 6Na + 3SO4
2Al + 6OH = 2Al(OH)3
7) Al(OH)3 +3HCl = 3H2O + AlCl3
Al(OH)3 + 3H + 3Cl = 3H2O + Al + 3Cl
Al(OH)3 + 3H = 3H2O + Al
8) AlCl3 + 4NaOH (избыток) = 3NaCl + Na[Al(OH)4]
Al + 3Cl + 4Na + 4OH = 3Na + 3Cl + Na + Al(OH)4
Al + 4OH = Al(OH)4
а) У кислорода: если он стоит один то 0 (это у всех, не только у кислорода)
также есть -2 (чаще всего в соединениях он проявляет такую степень окисления) ,
-1 в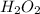 ,
,
+2 в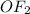 ,
,
так же может быть +4 в аллотропических модификациях кислорода.
б) У серы: -2 в сульфидах, гидросульфидах и сульфидокислотах,
если он стоит один то 0
+4 в тетрагалогенидах например,
+6 в соединениях с наиболее электроотрицательными элементами.
в) У азота: -3 в нитридах
-2 азот проявляет в соединениях перикисного типа,
в соединении под названием гидроксиламин он проявляет степень окисления -1
если он стоит один то 0
также может проявлять степени окисления +1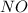 ,
, 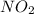 ,
,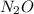
+3 и +5 в фториде, оксидах, оксогалогенидах.
г) Селенах: -2 в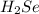 .
. 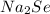
+4 селен проявляет в диоксиде, тетра- и оксогалогенидах
если он стоит один то 0
и в +6 это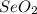 .
. 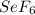
1) 2Al + 6HCl = 2AlCl3 + 3H2
2Al + 6H + 6Cl = 2Al + 6Cl + 6H
2) AlCl3 + 3NaOH = 3NaCl + Al(OH)3
Al + Cl3 + 3Na + 3OH = 3Na + 3Cl + Al(OH)3
Al + 3OH = Al(OH)3
3) 2Al(OH)3 = Al2O3 + 3H2O
2Al(OH)3 = 2Al + 3O + 3H2O
4) Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
2Al + 3O + 2Na + 2OH + 3H2O = 2Na + 2Al(OH)4
2Al + 3O + 2OH + 3H2O = 2Al(OH)4
5) 2Na[Al(OH)4] + 3Na2SO4 = Al2(SO4)3 + 8NaOH
2Na + 2Al(OH)4 + 6Na + 3SO4 = 2Al + 3SO4 + 8Na + 8OH
2Al(OH)4 = 2Al + 8OH
6) Al2(SO4)3 + 6NaOH = 2Al(OH)3 + 3Na2SO4
2Al + 3SO4 + 6Na + 6OH = 2Al(OH)3 + 6Na + 3SO4
2Al + 6OH = 2Al(OH)3
7) Al(OH)3 +3HCl = 3H2O + AlCl3
Al(OH)3 + 3H + 3Cl = 3H2O + Al + 3Cl
Al(OH)3 + 3H = 3H2O + Al
8) AlCl3 + 4NaOH (избыток) = 3NaCl + Na[Al(OH)4]
Al + 3Cl + 4Na + 4OH = 3Na + 3Cl + Na + Al(OH)4
Al + 4OH = Al(OH)4