На примере цинка и его соли поясните, какие свойства характерны для атомов и ионов металлов, окислительные или восстановительные. ответ сопроводите уравнениями реакций. К каждому уравнению реакции составьте электронный баланс В каких соединениях металлы находятся в природе? Что такое самородные металлы? Приведите примеры металлов, которые встречаются в самородном виде и только в соединениях.
Получение и изучение свойств основных классов неорганических веществ. Взаимосвязь различных классов веществ
Приведен следующий перечень реактивов: CuO, СuS, H2, Fe, HNO3, СuCl2.
Какие вещества из списка можно использовать, чтобы получить медь? Запишите молекулярные уравнения не менее двух реакций.
Напишите уравнения реакций восстановления оксидом углерода (II):
А) меди из Cu2O;
Б) кадмия из CdO;
В) марганца из Mn2O3.
Опишите экологические проблемы, которые могут возникнуть в непосредственной близости от металлургического комбината. Какие пути решения этих проблем можно предложить?
1 )оксид лития-Li2O
гидроксид натрия NaOH
Серная кислота - H2SO4
Оксид углерода - CO2
2 NaOH + H2SO4= Na2SO4 + 2 H2O
Li2O + H2SO4 = Li2SO4 + H2O
Li2O + CO2 = Li2CO3 ( при нагревании )
CO2 + 2 NaOH(избыток или расплав) = Na2CO3 + H2O
CO2(избыток) + NaOH = NaHCO3
2)
4 P+ 5 O2 = 2 P2O5 ( На самом деле: P4 (фосфор- белый) + 5 O2 = P4O10 P.S все немного сложнее) для общего развития реакция идет примерно так но в школе писать не советую, если интересно посмотрите )
P2O5 + H2O = H3PO4 ( опять же реакция для школьной химии )
3 KOH + H3PO4 = K3PO4 + 3 H2O
K3PO4 + Сa(OH)2 = Ca3(PO4)2↓ + KOH
Ca3(PO4)2 + 3 H2SO4 = 2 H3PO4 + 3 CaSO4
3)
фосфат алюминия- Al PO4
сульфид серебра - Ag2S
оксид марганца - MnO3
гидроксид магния Mn(OH)2
хлорид аммония NH4Cl
нитрат свинца (II) Pb (NO3)2
4)
a) Mg+ CuSO4 = MgSO4 + Cu
4 Mg + 5 H2SO4(концентрированная) = 4 MgSO4 + H2S↑ + 4 H2O
б) CaO+ H2O= Ca(OH)2
Ca(NO3)2 + KOH = KNO3 + Ca(OH)2↓
Ca + H3PO4 = Ca
5) 2AgNO3 + CuCl2 = 2AgCl↓ + Cu(NO3)2
Дано: Решение:
m(AgNO3) = 1,7 г n ( AgNO3) = m/M =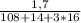 = 0,01 моль = n(AgCl)
= 0,01 моль = n(AgCl)
m ( AgCl) - ? m (AgCl)= n(AgCl) * M(AgCl)= 0,01 моль*
(108г/моль+35,5г/моль) = 1,435 г
ответ: 1,435 г
P.S. n- количество вещества ( еще обозначают как ν - "ню" )
6) CaO + H2SO4 = CaSO4 + H2O
Дано: n (CaO) - ?
m(H2SO4) = 14,7 г
n(H2SO4) = m/M = 14,7 г/ (2г/моль+32г/моль+4*16г/моль) = 0,15 моль=
= n(CaSO4)
m(CaSO4) = n*M = 0,15 моль*(40г/моль + 32г/моль+4*16г/моль)= 15,3 г
7)
Я не могу тут сделать нормальную таблицу, поэтому пусть это таблица : по горизонтали то что мы добавляем в пробирки по вертикали признаки реакции
----- | HNO3 | Ba(NO3)2
Na2CO3 | CO2↑ | помутнение воды
NaNO3 | -- | --
Na2SO4 | -- | осадок
Na2CO3 +2 HNO3 = H2O + CO2↑ + 2NaNO3
NaNO3 + HNO3 ≠
Na2SO4 + HNO3 ≠
Na2CO3 + Ba(NO3)2= BaCO3↓ + 2 NaNO3
Na2SO4 + Ba(NO3)2 = BaSO4↓ + 2 NaNO3
Нейтральную среду будут иметь соли, образованные сильным основанием и сильной кислотой. Разберем все соли в списке.
1) AICI3 - хлорид алюминия - образован слабым основанием (Al(OH)3) и сильной кислотой (HCl) - среда кислая
2) FeBr3 - бромид железа (ІІІ) - образован слабым основанием (Fe(OH)3) и сильной кислотой (HBr) - среда кислая
3) Na2SO4 - сульфат натрия - образован сильным основанием (NaOH) и сильной кислотой (H2SO4) - среда нейтральная
4) NaCl - хлорид натрия - образован сильным основанием (NaOH) и сильной кислотой (HCl) - среда нейтральная
5) FeSO4 - cульфат железа (ІІ) - образован слабым основанием (Fe(OH)2) и сильной кислотой (H2SO4) - среда кислая
ответ: 3 и 4