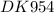N n =
A
ответ: N(H,0) = 6,622 - 1024.
Задача 3. Вычислите число атомов кислорода и водорода, которые
содержатся в 5 моль воды.
Дано:
Решение:
п(H,0) = 5 моль
= N = n N,
NA
N(O) - ?
Одна молекула воды состоит из одного ато-
N(Н) - ?
ма кислорода и двух атомов водорода. Отсюда
5 моль воды содержит 5 моль атомов кислорода
и 10 моль атомов водорода. Следовательно,
N(O) = 5 моль : 6,02 - 1023 моль-1 3,01 : 1024
N(H) = 10 : 6,02, 1023 = 6,02 : 1024
ответ: N(O) = 3,01 : 1024, N(H) = 6,02 - 1024.
55
ответ: w(NO)=0,7895; w(SiH4)=0,2105
Объяснение:
сумма электронов, протонов и нейтронов в молекуле оксида азота2:
7+7+7+8+8+8=45
сумма электронов и протонов в молекуле силана:
14+14+4+4=36
пусть n(газовой с-си)=1 моль, n(NO)=x моль, тогда n(SiH₄)=1-x моль
сумма всех электронов, протонов и нейтронов в оксиде азота2 будет равна произведению количества вещества на сумму электронов, протонов и нейтронов в молекуле на число молекул в 1 моль вещества(число Авогадро):
x*45*Nₐ=∑(NO)
аналогично для силана:
(1-x)*36*Nₐ=∑(SiH4)
составляем уравнение:
∑(NO)=5*∑(SiH4)
x*45*Nₐ=5*(1-x)*36*Nₐ
x=(1-x)*4
x=4-4x
x=4/5=0,8 -мольная доля NO в смеси
находим молярную массу смеси:
0,8*(14+16)+0,2*(28+4)=30,4 г/моль
массовая доля NO в смеси:
0,8*(14+16)/30,4=0,7895
массовая доля SiH4 в смеси:
1-0,7895=0,2105
Дано:
m(NaOH) = 42 гр
---------------------------
Найти:
m(OH⁻) - ?
1) Для начала запишем уравнение диссоциаций у гидроксида натрия, именно по такой уравнений реакций будет пользоваться:
NaOH → Na⁺ + OH⁻
2) Далее мы найдем количества вещества у гидроксида натрия а потом у иона гидроксида по уравнению реакций:
M(NaOH) = 23+16+1 = 40 гр/моль
n(NaOH) = m(NaOH) / M(NaOH) = 42 гр / 40 гр/моль = 1,05 моль ⇒ n(OH⁻) = n(NaOH) = 1,05 моль - по уравнению реакций
3) Теперь находим массу у иона гидроксида:
M(OH⁻) = 16+1 = 17 гр/моль
m(OH⁻) = n(OH⁻)×M(OH⁻) = 1,05 моль × 17 гр/моль = 17,85 гр ≈ 18 гр
ответ: m(OH⁻) = 18 гр
Решено от :