Мідь у промисловості отримують шляхом хімічної переробки куприту Сu2O або мідного блиску СuS. Які масові частки металу в кожній руді, та яку б з них ви запропонували для першочергової переробки?
А. Кислород располагается во 2 периоде и 6А (т.е. главной) подгруппе. порядковый номер - 8.
В. Любой природный атом кислорода содержит 8 протонов в ядре, но число нейтронов может быть равно 8, 9 или 10. (чаще всего встречается кислород с молярной массой 16, т.е. у него 8 протонов, 8 нейтронов и 8 электронов).
С. Электронная конфигурация атома кислорода в его основном состоянии:
D. Высшая -1(проявляется лишь в ряде веществ вроде перекиси водорода и прочих пероксидов, поэтому эта степень окисления, скорее, редкое исключение), низшая -2.
E. H2O2, Na2O2 (пероксид водорода и пероксид натрия)
n(CH4)= 10/16=0.625 моль
n(O2)=0.625*2=1.25 моль
m(O2)= 1.25*32=40 г
C2H4 + 3O2 = 2CO2 + 2H2O (t)
n(C2H4)= 10/28 = 0.36 моль
n(O2)=0.36*3=1.08 моль
m(O2)= 1.08*32= 34.56 г
2)а)
1) C + O2 = CO2 (t)
2) CO2 +H2O + CaCO3 <-> Ca(HCO3)2
3)Ca(HCO3)2 <-> CaCO3 + H2O + CO2
4)CaCO3 = CaO + CO2 (t)
б)
1) Zn + 2HCl= ZnCl2 + H2
2) ZnCl2 + 4NaOH= Na2ZnO2 + 2NaCl + 2H2O
3)Na2ZnO2 + 2HCl = Zn(OH)2 + 2NaCl
4)Zn(OH)2 = ZnO +H2O
в)
1) Mg + 2HCl = MgCl2 + H2
2) MgCl2(конц.) + H2O + MgO= 2MgOHCL
3)MgOHCl + HCl = MgCl2 + H2O
3) FeCl3 = Fe(3+) + 3Cl(-)
(SrOH)2СО3 = Sr(OH)2 (+) + CO3(2-)
NaH2PO4= Na (+) + H2PO4 (-)
Ca(OH)2 = Ca (2+) + 2OH(-)
А. Кислород располагается во 2 периоде и 6А (т.е. главной) подгруппе. порядковый номер - 8.
В. Любой природный атом кислорода содержит 8 протонов в ядре, но число нейтронов может быть равно 8, 9 или 10. (чаще всего встречается кислород с молярной массой 16, т.е. у него 8 протонов, 8 нейтронов и 8 электронов).
С. Электронная конфигурация атома кислорода в его основном состоянии: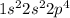
D. Высшая -1(проявляется лишь в ряде веществ вроде перекиси водорода и прочих пероксидов, поэтому эта степень окисления, скорее, редкое исключение), низшая -2.
E. H2O2, Na2O2 (пероксид водорода и пероксид натрия)
F. H2O, CaO.
Всего доброго.