К сплаву золота и серебра массой 10,4 г добавили2 л 0,24М раствора цианица натрия ( плотность = 1.07 г.мл) и барботировали воздух до полного растворения сплава. При этом масса раствора увеличилась на 10,52 г. Определить массовые доли всех веществ в полученном растворе.
Поскольку условия для каждой реакции не указаны, буду писать уравнение одной из возможных реакций.
Ba(OH)2+CuSO4= Cu(OH)2 + BaSO4
Ba(OH)2+Na2CO3= BaCO3 + 2NaOH
2KOH+H2CO3= K2CO3 + 2H2O
2HCL+CaCO3= CaCl2 + H2O + CO2
H2SO4+Zn= ZnSO4 + H2
H2SO4+CuO= CuSO4 + H2O
2HNO3+Cu(OH)2= Cu(NO3)2 + 2H2O
2H3PO4+3Ca(OH)2= Ca3(PO4)2 + 6H2O
NaOH+SO3= NaHSO4
2 HCL+K2CO3= 2KCl + H2O + CO2
H2SO4+Mg= MgSO4 + H2
3H2SO4+Fe2O3= Fe2(SO4)3 + 3H2O
HNO3+SiO2= хм... Такой реакции нет, насколько мне известно.
1) как водород простое вещество,связь неполярная.А валентность водорода равна |,то связь между атомами-одинарная
ОТВЕТ Г
2)Графическая(или структурная формула)Хлороводорода (HCl) выглядит так
4)H2+Br2→2HBr
H⁺+e⁻→H°(окиление,восстановитель)
Br¹-e⁻→Br°(восстановление,окислитель)
Значит,атом водорода ведет себя,как восстановитель,а атом брома-окислитель
5)
O2=ковалентно-неполярная связь
NH3=ковалентно-полярная связь
NaCl=ионная связь
6)
При действии окислителя не может происходить превращение из оксида железа FeO в железо Fe.
Запишем уравнение окислительно-восстановительной реакции (ОВР):
Водород H2 является восстановителем, а оксид железа FeO является окислителем. Значит, для перехода из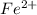 в
в 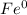 нужны восстановители
нужны восстановители