Химия 8 клас 1.определить валентности элементов по формуле вещества
a)AICI3 б)MgS в)SO3 r)N2O3
2.составить формулу сложных веществ состоящих из водорода и следущих химических элементов
а)азота3 в)кремня4
б)хлора1 г)серы2
3.раставить коэффициенты в уравнениях. Подчеркнуть формулу сложных веществ.Определить типы химических реакций
а)CuO+C=Cu+CO2
б)Fe+H2O=Fe3O4+H2
в)AI+O2=AI2O3
г)KNO3=KNO2+O2
а) У кислорода: если он стоит один то 0 (это у всех, не только у кислорода)
также есть -2 (чаще всего в соединениях он проявляет такую степень окисления) ,
-1 в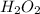 ,
,
+2 в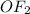 ,
,
так же может быть +4 в аллотропических модификациях кислорода.
б) У серы: -2 в сульфидах, гидросульфидах и сульфидокислотах,
если он стоит один то 0
+4 в тетрагалогенидах например,
+6 в соединениях с наиболее электроотрицательными элементами.
в) У азота: -3 в нитридах
-2 азот проявляет в соединениях перикисного типа,
в соединении под названием гидроксиламин он проявляет степень окисления -1
если он стоит один то 0
также может проявлять степени окисления +1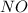 ,
, 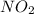 ,
,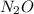
+3 и +5 в фториде, оксидах, оксогалогенидах.
г) Селенах: -2 в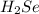 .
. 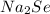
+4 селен проявляет в диоксиде, тетра- и оксогалогенидах
если он стоит один то 0
и в +6 это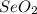 .
. 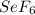
Периодический закон читается так: Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Периодическая система - это классификация химических элементов,устанавливающая зависимость различных свойств элементов от заряда атомного ядра.
Периодом называется горизонтальные ряды элементов таблицы Менделеева , в пределах которых свойства элементов изменяются последовательно.
Периодов в периодической системе 7,из них: а)малых-3;б)больших - 3 а в ) незаконченных только 1 седьмой
Малые периоды - это периоды который каждый из них состоит из одного горизонтального ряда,они имеют 10 элементов
В пределах малого периода с увеличением Ar постепенно изменяются свойства : а) металлические-уменьшаются а неметаллические увеличиваются.
Большие периоды-это периоды имеющие 18 и более элементов
С увеличением Ar изменение свойств химических элементов в больших периодах происходит так:
а)- в чётных рядах-(не знаю)
б) в нечётных рядах -(не знаю)
Группа элементов это последовательность атомов по возрастанию заряда ядра,обладающих однотипным электронным строением.
Высшая валентность по кислороду элементов одной группы соответствует номер группы
Главная подгруппа включает элементы литий, натрий, калий, рубидий и цезий, а также крайне нестабильный элемент франций.
Валентность элементов в водородных соединениях неметаллов определяется так:(не знаю как)
Побочная подгруппа включает элементы медь, серебро и золото, атомы которых имеют в предпоследнем слое по 18 электронов.