Химический диктант по теме: «Оксиды, кислоты, основания»
Вариант 11: оксид цинка.
Задание: Выберите верные утверждения (цифры), напишите уравнения возможных
химических реакций для вашего соединения с выбранными веществами.
Во Является основным компонентом природного минерала цинкита.
2. Является одним из «действующих лиц» проблемы кислотных осадков.
3. По составу - оксид металла.
4. По химическим свойствам - основный оксид.
5. По химическим свойствам - кислотный оксид.
6. В генетическом ряду ему соответствует кислотный гидроксид.
7. В генетическом ряду ему соответствует амфотерный гидроксид.
8. Образует два ряда солей.
9. Является полупроводником.
10. Обладает бактерицидными свойствами.
11. При обычных условиях - твердое кристаллическое вещество.
12. При обычных условиях - тяжелый газ.
13. Не имеет запаха.
14. Имеет резкий запах.
15. Имеет белый цвет.
16. Не имеет цвета.
17. Реагирует с водой.
18. Реагирует с гидроксидом натрия.
19. Реагирует с соляной кислотой.
20. Реагирует с углекислым газом (в соответствующих условиях).
21. Реагирует с оксидом бария.
22. Широко применяется в терапевтической стоматологии при создании
абразивных зубных паст и цементов.
23. В пищевой промышленности используется в качестве эмульгатора (пищевая
добавка Е529).
24. Используется для окуривания овощехранилищ и складских помещений с целью
дезинфекции.
25. Используется в строительстве при производстве силикатного кирпича.
26. Применяется в производстве стекла и керамики.
27. Используется для отбеливания соломы, шелка, шерсти.
28. Применяется в производстве искусственной кожи и резинотехнических
изделий.
29. Образуется при обжиге руды цинковой обманки.
30. Образуется при сжигании соответствующего вещества в атмосфере
кислорода.
Окислительно-восстановительные реакции– это реакции, сопровождающиеся переходом электронов от одних атомов или ионов к другим, другими словами – это реакции, в результате которых изменяются степени окисления элементов.
Степень окисления– это заряд атома элемента в соединении, вычисленный из условного предположения, что все связи в молекуле являются ионными.
Степень окисления принято указывать арабской цифрой над символом элемента со знаком плюс или минус перед цифрой. Например, если связь в молекуле HCl ионная, то водород и хлор ионы с зарядами (+1) и (–1), следовательно.
Для того чтобы рассчитать степень окисления любого элемента, необходимо пользоваться следующими правилами:
Степень окисления атомов в простых веществах равна нулю: (металл в свободном состоянии).Степень окисления (+1) во всех соединениях имеют щелочные металлы (IA группа) и водород, за исключением гидридов активных металлов, где степень окисления водорода равна (–1), например Степень окисления +2 во всех соединениях имеют щелочноземельные металлы (IIAгруппа).Кислород имеет степень окисления (–2), во всех соединениях, кроме пероксидов () и фторида кислорода.Алгебраическая сумма степеней окисления всех частиц в молекуле равна нулю, а в ионе – заряду иона → +1–1 = 0, .Степень окисления иона элемента равна заряду иона:Ca2+ + 2Cl1–.Не следует путать понятия «валентность» и «степень окисления». Так в N2, NH3, N2H4, NH2OH валентность (ковалентность) азота равна трем, так как азот образует три ковалентные связи, а степень окисления различна:
оксид серы (VI)
кислотный оксид
Степень окисления кислорода, как в любом оксиде, равна -2.
Степень окисления серы равна +6;
нитрат меди (II)
соль, имеет кисоую реакцию, так как гидролизуется по катиону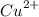 , как соль, образованная слабым основанием
, как соль, образованная слабым основанием 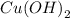 и сильной кислотой
и сильной кислотой 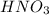 .
.
Cтепень окисления меди равна +2, степень окисления азота равна +5, степень окисления кислорода равна -2.
хлорат калия
нейтральная соль, поскольку образована сильными электролитами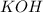 и
и 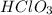
Степени окисления:
калий +1
хлор +5
кислород -2
фосфористая кислота, слабая
Степени окисления:
водород +1
фосфор +3
кислород -2