До розчину цинк сульфату масою 483 г із масовою часткою солі 5% додали розчин натрів гідроксидудо повного розчинення осаду. Обчисліть масу сполуки Цинку. 20,15 21,45 21,25 24,15
Конкурс «Учение с увлечением, или Как полюбить математику?»
Астрономия
Биология
Начальная школа
География
Иностранные языки
Информатика
История и обществознание
Краеведение
Литература
Математика
Музыка
МХК и ИЗО
ОБЖ
ОРКСЭ
Русский язык
Руководство учебным проектом
Спорт в школе и здоровье детей
Технология
Физика
Химия
Экология
Экономика
Администрирование школы
Видеоурок
Внеклассная работа
Дополнительное образование
Инклюзивное образование
Классное руководство
Коррекционная педагогика
Логопедия
Мастер-класс
Общепедагогические технологии
Организация школьной библиотеки
Патриотическое воспитание
Профессия — педагог
Работа с дошкольниками
Работа с родителями
Социальная педагогика
Урок с использованием электронного учебника
Школьная психологическая служба
Обратная связь
Многообразие решения задач на уроках химии
Собитнюк Любовь Васильевна, учитель
Разделы: Химия
Решение задач занимает в химическом образовании важное место, так как это один из приёмов обучения, посредством которого обеспечивается более глубокое и полное усвоение учебного материала и вырабатывается умение самостоятельного применения приобретённых знаний. Включение задач в учебный процесс позволяет уточнять и закреплять химические понятия о веществах и процессах, вырабатывать смекалку в использовании имеющихся знаний. Задачи побуждают учащихся повторять, углублять и осмысливать имеющиеся знания. В процессе решения задач воспитывается трудолюбие, целеустремлённость, развивается чувство ответственности, упорство и настойчивость в достижении поставленной цели. При решении задач реализуются межпредметные связи, показывается единство природы. В процессе решения задач идёт сложная мыслительная деятельность. Взаимодействие знаний и действий формированию разных приёмов мышления: суждений, умозаключений, доказательств.
Химические задачи можно решать устно, письменно и экспериментально, используя различные решения. Нельзя решать задачи от случая к случаю. Успех выработки умения решать задачи развивается, закрепляется при условии непрерывного решения задач на протяжении всего курса химии на основе созданной учителем определённой, постепенно усложняющейся системы. Как в природе всё гармонично, так и в решении задач должна быть своя гармония. Любая задача начинается с изучения её условия. Условия задач, если её нет в учебнике и сборнике задач, я предлагаю учащимся на карточках, чтобы они могли самостоятельно познакомиться с данными.
После изучения условия задачи, обязательно выясняем, с какими величинами предстоит проводить вычисления, устанавливаем единицы измерения и числовые значения данных задачи, чётко определяем искомую величину. Химические превращения записываем в виде уравнений реакций, расставляя коэффициенты перед формулами.
Решение любой задачи подобно сочинению музыки. Чтобы её сочинить, нужно знать ноты. Этими нотами в химии являются количественные соотношения. Взаимосвязь зависимости массы, объёма, числа частиц и теплового эффекта с количеством отражена на схеме:
Любые задачи можно решить несколькими Знакомство учащихся с разными позволяет им самим находить пути решения. Какой окажется более рациональным, ребята могут сравнить на уроке или в неурочное время, использую мультимедийный проектор. На примерах я покажу несколько решения задач.
Большинство задач, связанных с переходом от одного вещества к другому, мы решаем через количественные отношения. От нот к музыкальной фразе, точно так мы идём с учащимися при решении задач. Сначала отрабатываем количественные отношения в формулах, затем между веществами. На основе этого составляем схему решения задач на смеси веществ, между которыми нет взаимодействия:
Для решения такого типа задач используем схему
1. Смесь метана и этана массой 19 г занимает объём равный 16,8 л (при н. у.). Найти массовую или объёмную долю компонентов смеси.
Для решения многих задач используем несколько
1. Находим общее количество смеси: vсмеси=
vсмеси = = 0,75 моль
Используем схему перехода от количества к массе
2. Пусть vметана = х моль, vэтана= 0,75-х моль
mметана = 16х(г), mэтана= 30(0,75-х)
mметана+ mэтана= 19(г)
16х +30(0,75-х)=19
14х= 3,5
Х= 0,25моль
Так как мольная доля равна объёмной доли, следовательно:
vметана= = 0,333 или 33,3% img10.gif (64 bytes)этана= 66,7%
mметана = 4г, mэтана=15г.
Массовую долю веществ определяем по формуле:
img10.gif (64 bytes)
img10.gif (64 bytes)этана== 0,78,9 или 78,9%, img10.gif (64 bytes)метана= 11,1%
1. Находим общее количество смеси: vсмеси=
vсмеси = = 0,75 моль
2. Пусть х г- масса метана, (18-х)г - масса этана.
Дано:
n(Zn) = 0,2 моль
Найти:
m(Zn) - ?
n =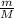 ⇒ m = n * M
⇒ m = n * M
M(Zn) = Ar(Zn) = 65 г/моль
m(Zn) = 0,2 моль * 65 г/моль = 13 г.
ответ: m(Zn) = 13 г.2)Дано:
N(MgO) = 3 * 10²³ частиц
Найти:
m(MgO) - ?
n(MgO) - ?
n(MgO) = =
=  ≈ 0,5 моль
≈ 0,5 моль
m(MgO) = n * M
M(MgO) = Ar(Mg) + Ar(O) = 24 * 16 = 40 г/моль
m(MgO) = 0,5 моль * 40 г/моль = 20 г.
ответ: n(MgO) ≈ 0,5 моль, m(MgO) = 20 г.3)Дано:
m(CO₂) = 22 г.
Найти:
n(CO₂) - ?
N(CO₂) - ?
n(CO₂) =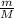
M(CO₂) = Ar(C) + Ar(O) * 2 = 12 + 16 * 2 = 12 + 32 = 44 г/моль
n(CO₂) = 22 г. / 44 г/моль = 0,5 моль
N(CO₂) = n * N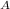 = 0,5 моль * 6,02 * 10²³ моль⁻¹ = 3,01 * 10²³ частиц
= 0,5 моль * 6,02 * 10²³ моль⁻¹ = 3,01 * 10²³ частиц
ответ: n(CO₂) = 0,5 моль, N(CO₂) = 3,01 * 10²³ частиц.4)Дано:
N(Br₂) = 12 * 10²³ частиц
Найти:
m(Br₂) - ?
n(Br₂) - ?
n(Br₂) = =
= 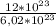 ≈ 2 моль
≈ 2 моль
m(Br₂) = n * M
M(Br₂) = Ar(Br) * 2 = 80 * 2 = 160 г/моль
m(Br₂) = 2 * 160 = 320 г.
ответ: n(Br₂) = 2 моль, m(Br₂) = 320 г.5)Дано:
m(H₂SO₄) = 98 г.
Найти:
N(H₂SO₄) - ?
n(H₂SO₄) - ?
n(H₂SO₄) =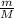
M(H₂SO₄) = Ar(H) * 2 + Ar(S) + Ar(O) * 4 = 1 * 2 + 32 + 16 * 2 = 2 + 32 + 32 =
68 г/моль
n(H₂SO₄) = 98 г. / 68 г/моль ≈ 1,5 моль
N(H₂SO₄) = n * N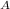 = 1.5 моль * 6,02 * 10²³ моль⁻¹ = 9,03 частиц
= 1.5 моль * 6,02 * 10²³ моль⁻¹ = 9,03 частиц
ответ: n(H₂SO₄) ≈ 1,5 моль, N = 9,03 частицОткрытый урок | Первое сентября
Главная
Положение о фестивале и конкурсах
Поиск по сайту
Статья недели
Разделы
Конкурс «Презентация к уроку»
Конкурс «Путь к Великой Победе»
Конкурс «Волонтерское движение в школе»
Конкурс «Мы мир храним, пока мы помним о войне»
Конкурс «История регионов России»
Конкурс по экологии «Земля — наш общий дом»
Конкурс «Цифровой класс»
Конкурс «Электронный учебник на уроке»
Конкурс «Учение с увлечением, или Как полюбить математику?»
Астрономия
Биология
Начальная школа
География
Иностранные языки
Информатика
История и обществознание
Краеведение
Литература
Математика
Музыка
МХК и ИЗО
ОБЖ
ОРКСЭ
Русский язык
Руководство учебным проектом
Спорт в школе и здоровье детей
Технология
Физика
Химия
Экология
Экономика
Администрирование школы
Видеоурок
Внеклассная работа
Дополнительное образование
Инклюзивное образование
Классное руководство
Коррекционная педагогика
Логопедия
Мастер-класс
Общепедагогические технологии
Организация школьной библиотеки
Патриотическое воспитание
Профессия — педагог
Работа с дошкольниками
Работа с родителями
Социальная педагогика
Урок с использованием электронного учебника
Школьная психологическая служба
Обратная связь
Многообразие решения задач на уроках химии
Собитнюк Любовь Васильевна, учитель
Разделы: Химия
Решение задач занимает в химическом образовании важное место, так как это один из приёмов обучения, посредством которого обеспечивается более глубокое и полное усвоение учебного материала и вырабатывается умение самостоятельного применения приобретённых знаний. Включение задач в учебный процесс позволяет уточнять и закреплять химические понятия о веществах и процессах, вырабатывать смекалку в использовании имеющихся знаний. Задачи побуждают учащихся повторять, углублять и осмысливать имеющиеся знания. В процессе решения задач воспитывается трудолюбие, целеустремлённость, развивается чувство ответственности, упорство и настойчивость в достижении поставленной цели. При решении задач реализуются межпредметные связи, показывается единство природы. В процессе решения задач идёт сложная мыслительная деятельность. Взаимодействие знаний и действий формированию разных приёмов мышления: суждений, умозаключений, доказательств.
Химические задачи можно решать устно, письменно и экспериментально, используя различные решения. Нельзя решать задачи от случая к случаю. Успех выработки умения решать задачи развивается, закрепляется при условии непрерывного решения задач на протяжении всего курса химии на основе созданной учителем определённой, постепенно усложняющейся системы. Как в природе всё гармонично, так и в решении задач должна быть своя гармония. Любая задача начинается с изучения её условия. Условия задач, если её нет в учебнике и сборнике задач, я предлагаю учащимся на карточках, чтобы они могли самостоятельно познакомиться с данными.
После изучения условия задачи, обязательно выясняем, с какими величинами предстоит проводить вычисления, устанавливаем единицы измерения и числовые значения данных задачи, чётко определяем искомую величину. Химические превращения записываем в виде уравнений реакций, расставляя коэффициенты перед формулами.
Решение любой задачи подобно сочинению музыки. Чтобы её сочинить, нужно знать ноты. Этими нотами в химии являются количественные соотношения. Взаимосвязь зависимости массы, объёма, числа частиц и теплового эффекта с количеством отражена на схеме:
Любые задачи можно решить несколькими Знакомство учащихся с разными позволяет им самим находить пути решения. Какой окажется более рациональным, ребята могут сравнить на уроке или в неурочное время, использую мультимедийный проектор. На примерах я покажу несколько решения задач.
Большинство задач, связанных с переходом от одного вещества к другому, мы решаем через количественные отношения. От нот к музыкальной фразе, точно так мы идём с учащимися при решении задач. Сначала отрабатываем количественные отношения в формулах, затем между веществами. На основе этого составляем схему решения задач на смеси веществ, между которыми нет взаимодействия:
Для решения такого типа задач используем схему
1. Смесь метана и этана массой 19 г занимает объём равный 16,8 л (при н. у.). Найти массовую или объёмную долю компонентов смеси.
Для решения многих задач используем несколько
1. Находим общее количество смеси: vсмеси=
vсмеси = = 0,75 моль
Используем схему перехода от количества к массе
2. Пусть vметана = х моль, vэтана= 0,75-х моль
mметана = 16х(г), mэтана= 30(0,75-х)
mметана+ mэтана= 19(г)
16х +30(0,75-х)=19
14х= 3,5
Х= 0,25моль
Так как мольная доля равна объёмной доли, следовательно:
vметана= = 0,333 или 33,3% img10.gif (64 bytes)этана= 66,7%
mметана = 4г, mэтана=15г.
Массовую долю веществ определяем по формуле:
img10.gif (64 bytes)
img10.gif (64 bytes)этана== 0,78,9 или 78,9%, img10.gif (64 bytes)метана= 11,1%
1. Находим общее количество смеси: vсмеси=
vсмеси = = 0,75 моль
2. Пусть х г- масса метана, (18-х)г - масса этана.