Часть 1. Дана схема превращений P-> P205-> Ca;(PO4)2
1. Составьте уравнения химических реакций
2. Расставьте степени окисления всех химических элементов
3. Назовите все вещества
4. Укажите фазовые состояния веществ
5. Укажите тип каждой реакции ( соединение, разложение, обмен, замещение, экзо-
эндотермические, каталитические или некаталитические)
6. Укажите вид химический связи для веществ, используемых в уравнениях реакции (
металлическая, ионная, ковалентная полярная или ковалентная неполярная)
7. Укажите тип кристаллической решетки для веществ, используемых в уравнении (
металлическая, ионная, молекулярная, атомная)
8. Для всех веществ укажите, являются ли они электролитами или неэлектролитами
9. для 1 реакции составьте электронный баланс, укажите окислитель и
восстановитель
10. Для реакции ионного обмена составьте полное и сокращенное ионное уравнение.
Часть 2 Решите задачу. Определите массу гидроксида индия( III) , полученного при взаимодействии 200г 15% раствора нитрата индия( ПП с гидроксидом натрия.
1) Уравняем схему рекации:
Из чего можно сделать вывод о том, что KCl образуется столько же, сколько KClO3 было. А O2 в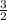 раза больше, поэтому.
раза больше, поэтому.
2) 3 Ba + 2 H3PO4 → 3 H2 + Ba3(PO4)2
Бария столько же, сколько и водорода, следовательно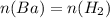
Фосфорной кислоты 3/4 от количества водорода
3) Поскольку 4,8% примесей, то
1000г*0,048=48 грамм примесей.
Тогда чистого железа
1000 - 48 = 952 г.
Fe+H2SO4 => FeSO4 + H2
n(Fe)=m/M=952/56=17 моль
Соли образуется столько же, сколько и железа было
n(Fe)=n(FeSO4)
m(FeSO4)=n*M = 17*152 = 2584 г
Водорода образуется столько же, поэтому
n(Fe)=n(H2)
V(H2)=n*Vm = 17* 22,4 = 380,8 л.
В первом периоде у водорода всего 1 s электрон, у гелия - 2 s электроны. В дальнейшем на первой орбитали всегда будет два электрона.
На второй уровне 3 орбитали:
первая орбиталь 2 s электрона, вторая орбиталь 2 s электрона и идет постепенное заполнение p -электронов до 6.
На третьем уровне:
3 орбитали: первая орбиталь 2 s электрона, вторая орбиталь 2 s электрона и 6 p -электронов. Появляется третья орбиталь на которой в третье уровне пока нет электронов. В ДАЛЬНЕЙШЕМ НА НЕЙ МОЖЕТ БЫТЬ 10 ЭЛЕКТРОНОВ.
Объяснение: