1.В каком соединении ст.окисления углерода равна 0?
1)CO 2)CH4 3)CCE4 4)CH3CE
5)CH2CE2
2.Определите степени оксиления хлора в соединениях: CE2O,NaCE,CE2,SCE2,CE2O3,HCE
3.Укажите валентность и степени окисления азота в нитрат-ионе (NO3-)
4.Завершите процессы
1. Запах альдегида:
C2H5OH =CuO= Cu + CH3COH + H2O
Реакция серебрянного зеркала
HCOOH + 2[Ag(NH3)2]OH = 2Ag + CO2 + 2H2O + 4NH3
2. Если процесс происходит при нагревании, то появляется ярко-оранжевое окрашивание - оксид меди.
C6H12O6 + 2Cu(OH)2(t) = C6H12O7 + Cu2O + 2H2O
в пробирке с глицерином с гидроксидом меди образуется темно-синий раствор - во вложении
3. На белок биуретова проба - во вложении реакция
Если к формальдегиду добавить щелочь и сульфат меди, а потом слегка подогреть появится оранжевый осадок оксида одновалентной меди.
CuSO4 + 2NaOH ---> Cu(OH)2 + Na2SO4
R-CHO + 2Cu(OH)2 (t) ---> R-COOH + Cu2O + 2H2O
4. Растительные масла это эфиры глицерина и жирных непредельных кислот, поэтому они легко омыляются щелочью, при температуре 250 С и выше разлагаются на акролеин и жирные кислоты с неприятным запахом.
Минеральные масла в основном состоят из предельных углеводородов С18Н38 и выше. Они не омыляются щелочами и не разлагаются при температуре.
5. Реакция на крахмал - с йодом дает синее окрашивание.
6. Описаны реакции
7. Сахароза не дает реакций серебряного зеркала и с гидроксидом меди в отличие от глюкозы
1. Сначала найдем относительную молекулярную массу оксида:
2. Теперь допустим,что валентность элемента в оксиде равно I, тогда формула оксида -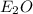 , подставив в формулу по вычислению молекулярной массы,получим уравнение:
, подставив в формулу по вычислению молекулярной массы,получим уравнение:
Химический элемент с относительной атомной массой 14 - это Азот, значит формула оксида: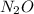 , т.е. оксид азота(I) или так называемый "веселильный газ",который долгое время использовали как анастезирующее
, т.е. оксид азота(I) или так называемый "веселильный газ",который долгое время использовали как анастезирующее
3. Теперь допустим,что элемент 4-х валентный,тогда формула оксида -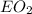 ?получим уравнение:
?получим уравнение:
Химический элемент с относительной атомной массой 12 - Углерод,а формула оксида -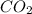 , т.е. оксид углерода(IV) или углекислый газ
, т.е. оксид углерода(IV) или углекислый газ