1. к окислительно-восстановительным реакциям не относится реакция?
1)cu+hno3 -> cu(no3)2+h2o+no2
2)cuo+p2o5-> cu3(po4)2
3)cuo+h2-> cu+h2o
4)cu+h2so4-> cuso4+h2o+so2
2.установите соответствие между окислительно-восстановительным процессом,обозначенным схемой передачи электронов,и схемой реакции.
-2 0
1) s-> s a.hno3-> h2o+no2+o2
+6 +4 б.h2s+so2-> h2o+s
2)s-> s в.nh3+o2-> h2o+no
+5 +4 г.nh3+o2-> h2o+n2
3)n-> n д.c+h2so4-> co2+so2+h2
-3 0
4)n-> n
х л 149 г
67,2 л 149 г
1. Сначала необходимо определить теоретически возможную массу ортофосфата:
111,75 г - это 75%,а
у г_________100%, откуда у=111,75*100/75=149 г
2. Подставив данную массу в уравнение,получим:
при взаимодействии 67,2 л аммиака получится 149 г аммоний ортофосфата,а
при -- // -- х л____________________149 г, откуда,глядя на пропорцию,видим,что такой же объем и необходим,т.е. 67,2 л
Слушай, по-моему, здесь осуществимы только три реакции реакции (а, б, в), поскольку это зависит от атомов водорода в данном веществе. А в данном веществе, т.е в фосфорной (ортофосфорной) кислоте, по количеству- 3 атома водорода. Ландо, давай проведём осуществимые реакции:
а)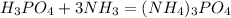 - Как удобрение: нигде не слышал, чтобы их как-то специфически называли. Вроде, ортофосфаты и есть ортофосфаты! Как продукт: Ортофосфат аммония;
- Как удобрение: нигде не слышал, чтобы их как-то специфически называли. Вроде, ортофосфаты и есть ортофосфаты! Как продукт: Ортофосфат аммония;
б)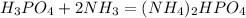 - Как удобрение: диаммофос; Как продукт: Гидроортофосфат аммония;
- Как удобрение: диаммофос; Как продукт: Гидроортофосфат аммония;
в)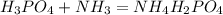 - Как удобрение: Аммофос - с примесями
- Как удобрение: Аммофос - с примесями 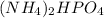 ; Как продукт: Дигидроортофосфат аммония; Вот, вроде так.
; Как продукт: Дигидроортофосфат аммония; Вот, вроде так.
Естественно, это сложные вещества, потому что состоят они из атомов разных химических элементов, в данном случае, это водород, фосфор, азот, кислород. Тебе для заметки: Простое вещество состоит из атомов одного химического элемента (Кислород, сера, водород). А сложное- из атомов разных химических элементов (Тот же ортофосфат аммония). Всё!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Щёлк Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."