1 из 1
Тема: « Щелочные металлы».
Часть А
А 1. Сколько электронов содержат на внешнем энергетическом уровне атомы щелочных металлов:
а) два б) один в) три г) четыре
А 2. В химических реакциях металлический натрий проявляет:
а) окислительные свойства б) восстановительные свойства
в) кислотные свойства г) основные свойства
А 3. В ряду химических элементов Na→K→Rb→Cs→Fr металлические свойства:
а) усиливаются б) ослабевают
в) не изменяются г) изменяются периодически
А 4. Соединения щелочных металлов с водородом называется:
а) галогениды б) гидроксиды в) гидриды г) нитриды
А5. Карбонат какого щелочного металла имеет техническое название «поташ»:
а) натрия б) калия в) лития г) цезия
А 6При взаимодействии щелочноземельных металлов с водой образуютя…
1) гидриды и кислород
2) основания и водород
3) пероксиды и водород
А 7Металлы I I группы главной подгруппы будут взаимодействовать с кислотами те, …
1) которые в ряду напряжения металлов стоят после Н
2) которые в ряду напряжения металлов стоят до Н
3) будут реагировать все
А 8. Оксиды щелочноземельных металлов имеют общую молекулярную формулу…
1) МеО2
2) МеО
3) Ме2О
А 9.задание: Осуществите превращения, запишите соответствующие уравнения реакций.
Мq СО3 → МqСl2 → Мq (ОН)2→ МqО →Мq
А. 10 задание: закончите уравнения реакций
а) Са + Н2О →
б) Са(ОН)2 + СО2 →
Часть Б (на выбор одно задание)
Б 1. Закончите уравнения реакций, характеризующие химические свойства металла. Дайте название продуктам реакции.
1) Сa + Cl2 =
2) Сa + O2 =
3) Сa + H2 =
4) Сa + S =
5) Сa + N2 =
6)Сa + H2O =
Часть С
Решите задачу:
Какой объем кислорода потребуется для его взаимодействия с натрием количеством вещества 0,3 моль?
Коллоидные системы отличие от истинных растворов
Как показали многочисленные исследования, коллоидные системы по своим молекулярно-кинетическим свойствам принципиально ничем не отличаются от обычных (истинных) растворов, только эти свойства у золей и растворов высокомолекулярных соединений выражены значительно (в сотни и тысячи раз) слабее. [c.299]
Нефть и нефтяные остаточные фракции содержат в своем составе различные высокомолекулярные соединения, которые при определенных условиях склонны к взаимодействию с образованием комбинаций, очевидно, более крупного размера, чем единичная их составляющая. В этом случае нефтяные системы находятся в коллоидном состоянии, то есть представляют собой дисперсные системы, в которых отдельные частицы являются не молекулами, а комбинациями, состоящими из множества молекул. Состав этих комбинаций может быть либо постоянным во времени, либо непрерывно изменяться в зависимости от термобарических и других условий существования нефтяной системы. Такие системы сильно отличаются от истинных растворов
1) Уравняем схему рекации:
Из чего можно сделать вывод о том, что KCl образуется столько же, сколько KClO3 было. А O2 в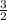 раза больше, поэтому.
раза больше, поэтому.
2) 3 Ba + 2 H3PO4 → 3 H2 + Ba3(PO4)2
Бария столько же, сколько и водорода, следовательно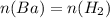
Фосфорной кислоты 3/4 от количества водорода
3) Поскольку 4,8% примесей, то
1000г*0,048=48 грамм примесей.
Тогда чистого железа
1000 - 48 = 952 г.
Fe+H2SO4 => FeSO4 + H2
n(Fe)=m/M=952/56=17 моль
Соли образуется столько же, сколько и железа было
n(Fe)=n(FeSO4)
m(FeSO4)=n*M = 17*152 = 2584 г
Водорода образуется столько же, поэтому
n(Fe)=n(H2)
V(H2)=n*Vm = 17* 22,4 = 380,8 л.