1. Алканы. Гомологический ряд, номенклатура, изомерия углеродного скелета, 2. Перечислите названия десяти первых представителей гомологического ряда.3. Перечислите основные правила построения названий предельных углеводородов по номенклатуре ИЮПАК. Пр Проиллюстрируйте их на конкретном примере. 3А. Написать формулы веществ: 2метилбутан, 2,3диметилпентан, 3,3диметилгексан. Написать и назвать все изомеры гексана.4. Химические свойства алканов: галогенирование, горение, термическое превращение (разложение, дегидрирование). Приведите реакции на примере этана. 5. Даны вещества: 02, H2, Br2, H20, C12. С какимиз них будет взаимодействовать пропан? Запишите уравнения химических реакций.6. Получение алканов 7.Алкены. Гомологический ряд, номенклатура, изомерия углеродного скелета положения двойной связи в молекуле. 8.На примере пентена покажите основные типы изомерии алкенов и правила номенклатуры ИЮПАК
2,2,3,3,4-пентаметилпентан 2,2,3,3-тетраметилгексан 2,2,3,4,4-пентаметилпентан 2,2,3,4-тетраметилгексан 2,2,3,5-тетраметилгексан 2,2,3-триметил-3-этилпентан 2,2,3-триметилгептан 2,2,4,4-тетраметилгексан 2,2,4,5-тетраметилгексан 2,2,4-триметил-3-этилпентан 2,2,4-триметилгептан 2,2,5,5-тетраметилгексан 2,2,5-триметилгептан 2,2,6-триметилгептан 2,2-диметил-3-этилгексан 2,2-диметил-4-этилгексан 2,2-диметилоктан 2,3,3,4-тетраметилгексан 2,3,3,5-тетраметилгексан 2,3,3-триметилгептан 2,3,4,4-тетраметилгексан 2,3,4-триметил-3-этилпентан 2,3,4-триметилгептан 2,3,5-триметилгептан 2,3,6-триметилгептан 2,3-диметил-3-этилгексан 2,3-диметил-4-этилгексан 2,3-диметилоктан 2,4,4-триметилгептан 2,4,5-триметилгептан 2,4,6-триметилгептан 2,4-диметил-3-этилгексан 2,4-диметил-4-этилгексан 2,4-диметилоктан 2,5,5-триметилгептан 2,5-диметил-3-этилгексан 2,5-диметилоктан 2,6-диметилоктан 2,7-диметилоктан 2-метил-3,3-диэтилпентан 2-метил-3-этилгептан 2-метил-4-этилгептан 2-метил-5-этилгептан 2-метилнонан 3,3,4,4-тетраметилгексан 3,3,4-триметилгептан 3,3,5-триметилгептан 3,3-диметил-4-этилгексан 3,3-диметилоктан 3,3-диэтилгексан 3,4,4-триметилгептан 3,4,5-триметилгептан 3,4-диметил-3-этилгексан 3,4-диметилоктан 3,4-диэтилгексан 3,5-диметилоктан 3,6-диметилоктан 3-изопропил-2,4-диметилпентан 3-изопропил-2-метилгексан 3-метил-3-этилгептан 3-метил-4-этилгептан 3-метил-5-этилгептан 3-метилнонан 3-этилоктан 4,4-диметилоктан 4,5-диметилоктан 4-изопропилгептан 4-метил-3-этилгептан 4-метил-4-этилгептан 4-метилнонан 4-пропилгептан 4-этилоктан 5-метилнонан н-декан
Источник: https://gomolog.ru/baza-znanii/strukturnye-formuly/2,3,4,5-tetrametilgeksan.html
Объяснение:
1. Докажите опытным путём состав: а) гидроксида кальция; б) сульфата аммония.
а) Проведём качественную реакцию на гидроксид-ион. Для этого воспользуемся индикаторами. Гидроксид кальция - основание малорастворимое, но тем не менее некоторое количество растворяется, следовательно среду изменять будет. Возьмём индикатор фенолфталеин, добавим его в пробирку с гидроксидом кальция, в результате раствор частично изменит цвет на малиновый - следовательно среда щелочная (слабощелочная).
б) Проведём качественную реакцию на сульфат-ион. Для этого возьмём любую растворимую соль бария (по стандарту - хлорид бария), добавим его в раствор с сульфатом аммония. В ходе реакции выпадает белый осадок - сульфат бария. Реакция выглядит следующим образом:
ᅠᅠ
2. Испытайте растворы нитрата натрия, карбоната натрия и нитрата цинка раствором индикатора или индикаторной бумагой, и объясните результаты испытаний. Запишите молекулярные и ионные уравнения реакций гидролиза:
1. Нитрат натрия - соль, образованная сильным основанием NaOH и сильной кислотой HNO₃, гидролиз протекать не будет, среда нейтральная. Это можно доказать следующим путём: возьмём индикатор метиловый оранжевый, добавим его в раствор нитрата натрия, в результате цвет изменится на оранжевый. Это и есть признак нейтральной среды.
2. Карбонат натрия - соль, образованная сильным основанием NaOH и слабой кислотой H₂CO₃. Гидролиз протекает по аниону, образующаяся среда - щелочная, гидролиз обратимый, протекает в две стадии:
ᅠᅠ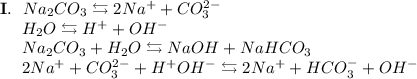
ᅠᅠ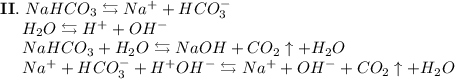
Добавим в раствор метиловый оранжевый. Раствор поменяет цвет на жёлтый, следовательно реакция среды щелочная.
3. Нитрат цинка - соль, образованная слабым основанием Zn(OH)₂ и сильной кислотой HNO₃. Гидролиз протекает по катиону, образующаяся среда - кислая, гидролиз обратимый, протекает в две стадии:
ᅠᅠ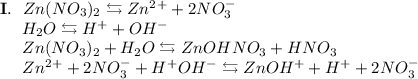
ᅠᅠ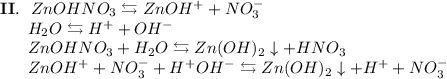
Добавим в раствор метиловый оранжевый. Раствор поменяет цвет на красный, следовательно реакция среды кислая.
3. Практически осуществите все следующие превращения: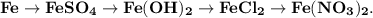
1. Получим сульфат железа путём реакции железа и разбавленной серной кислоты:
ᅠᅠ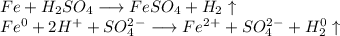
С точки зрения ОВР:
ᅠᅠ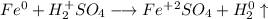
ᅠᅠ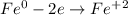 | 2 | 1 | окисление
| 2 | 1 | окисление
ᅠᅠ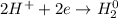 | 2 | 1 | восстановление
| 2 | 1 | восстановление
ᅠᅠFe - восстановитель, H₂SO₄ (2H⁺) - окислитель.
2. Получим гидроксид железа путём реакции сульфата железа и гидроксида калия:
ᅠᅠ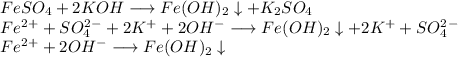
3. Получим хлорид железа путём реакции гидроксида железа и хлороводородной кислоты:
ᅠᅠ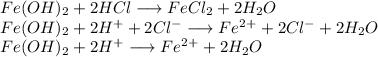
4. Получим нитрат железа путём реакции хлорида железа и азотной кислоты: